 En radiología, la atenuación se refiere a una reducción en el número de energía de fotones en hay de rayos-X. La atenuación, por tanto, es una reducción en la intensidad de un haz de rayos-X. En gran medida, la atenuación de rayos-X está determinada por la densidad del tejido; la diferencia en las densidades tisulares es responsable de la creación de imágenes vistas con los rayos-X, por lo que mientras más denso el tejido, más electrones contiene. El número de electrones en el tejido determina la habilidad del tejido para atenuar o transmitir los fotones en el haz de rayos-X. Las diferencias en la patrón de los fotones transmitidos o atenuados crean el contraste necesario para discernir imágenes en los rayos-X.
En radiología, la atenuación se refiere a una reducción en el número de energía de fotones en hay de rayos-X. La atenuación, por tanto, es una reducción en la intensidad de un haz de rayos-X. En gran medida, la atenuación de rayos-X está determinada por la densidad del tejido; la diferencia en las densidades tisulares es responsable de la creación de imágenes vistas con los rayos-X, por lo que mientras más denso el tejido, más electrones contiene. El número de electrones en el tejido determina la habilidad del tejido para atenuar o transmitir los fotones en el haz de rayos-X. Las diferencias en la patrón de los fotones transmitidos o atenuados crean el contraste necesario para discernir imágenes en los rayos-X.
Por lo anterior, si todos los fotones fueran atenuados (o ninguno fuera trasmitido), no se vería imagen porque la película sería totalmente blanca. Si todos los fotones fueran transmitidos (o ninguno fuera atenuado) no se vería imagen porque la película sería totalmente negra. La diferencia en la atenuación de la energía de fotones de los rayos-X por los diferentes tejidos es responsable del contraste en una placa de rayos-X, lo que permite que las imágenes sean vistas. Si el grado de atenuación puede ser cuantificado, sería posible valorar cuantitativamente la densidad del tejido también. Esta es la premisa detrás de la medición de densidad ósea (o de otros tejidos) con las técnicas absorciométricas de fotones.
Las técnicas tempranas de absorciometría de fotones empleaban radionúclidos para generar energía de fotones. Estas técnicas basadas en radionúclidos han cedido el paso a las técnicas basadas en rayos-X, aunque los principios básicos por los que operan siguen siendo los mismos.
Absorciometría de fotón único
En 1963 se describió un nuevo método para determinar la densidad ósea in vivo, pasando un haz de fotones monocromático o de energía única a través del hueso y el tejido blanco. La cantidad de mineral encontrado por el haz podría ser cuantificado por sustracción de la intensidad del haz después de pasar por la región de interés de la intensidad inicial de dicho haz. En estas unidades tempranas de absorciometría de fotón único (SPA, por sus siglas en inglés), los resultados de múltiples pases de escaneo en una sola ubicación, usualmente el radio medio, eran promediadas. En las unidades más recientes, los pases de escaneo a intervalos equidistantes a lo largo del hueso fueron utilizados, de manera que la masa de mineral por unidad de longitud de hueso pudiera ser calculada. Un detector de cintilación era utilizado para cuantificar la energía de fotones después de la atenuación por el hueso y el tejido blanco en la ruta de escaneo. Luego de cuantificar la atenuación de fotones, una comparación con la atenuación de fotones vista con un estándar de calibración derivado de hueso humano seco y sin grasa, de peso conocido, era realizada a fin de determinar la cantidad de mineral óseo.
El haz de fotones y el detector eran altamente colimado (se dice que un haz de luz está colimado si la divergencia del vector de Poynting correspondiente es nula) o restringido en tamaño y forma. La fuente del haz y el detector se movían en tándem a través de la región de interés, unidos por un sistema mecánico. Originalmente se empleaba 125I a 27.3 keV o 241Am a 59.6 keV para generar el haz de fotones de energía única, aunque la mayoría de las unidades SPA subsecuentes emplearon solamente 125I.
Los cálculos físicos para las determinaciones SPA del mineral óseo eran válidos solamente cuando había un espesor uniforme del hueso y tejido blanco en la ruta de escaneo. A fin de crear artificialmente este tipo de espesor uniforme, la extremidad a ser estudiada debía ser sumergida en un baño de agua o rodeada por un material equivalente al tejido. Esto limitaba la SPA a mediciones del esqueleto apendicular distal tales como radio y calcáneo.
La absorciometría de fotón único era tanto exacta como precisa, aunque los parámetros variaban ligeramente con el sitio estudiado. Para mediciones SPA del radio medio, la exactitud variaba del 3% al 5% y la precisión del 1% al 2%. Mediciones tempranas del radio distal y ultradistal con SPA no demostraron el mismo grado de precisión, debido primariamente a cambios marcados en la composición del hueso con muchos pequeños cambios de localización dentro del radio distal y ultradistal. Con los últimos instrumentos, que emplearon rutinas de localización mejoradas por computadora y escaneo rectilíneo, las mediciones SPA del radio distal y ultradistal se acercaron a una precisión del 1%. La exactitud y precisión de las mediciones del calcáneo con SPA fueron reportadas como menores a 3%. La dosis de radiación dérmica para el radio y el calcáneo fue de 5.10 mrem, aunque la dosis de radiación biológicamente importante, la dosis efectiva, era insignificante. Los resultados eran reportados como contenido mineral óseo (BMC, por sus siglas en inglés) en gramos o como contenido mineral óseo por unidad de longitud (BMD/l, por sus siglas en inglés) en gramos/centímetro. El tiempo requerido para realizar dichos estudios era aproximadamente de 10 minutos.
SPA es raramente realizada en la actualidad, habiendo sido reemplazada primero por la absorciometría de rayos-X de energía única (SXA, por sus siglas en inglés) y luego por la absorciometría de rayos-X de energía dual (DXA, por sus siglas en inglés). La desaparición de SPA fue debida a mejoras en la facilidad de uso y en la precisión obtenida con SXA y DXA. SPA fue una tecnología exacta que podría ser usada para predecir el riesgo de fractura; la habilidad para predecir el riesgo de fracturas apendiculares con mediciones SPA del radio fue establecida convincentemente. Las mediciones SPA del radio fueron también buenos predictores de riesgo de fractura de columna y riesgo global de fractura. Las pruebas de fractura más amplias publicadas demostraron la habilidad de una sola medición de masa ósea para predecir fracturas, empleando mediciones SPA del radio.
Absorciometría de fotón dual
El principio básico involucrado en la absorciometría de fotón dual (DPA, por sus siglas en ingles) para la medición de densidad ósea, fue la misma que para la absorciometría de fotón único; cuantificar el grado de atenuación de un haz de energía de fotones después de pasar a través de tejido óseo y tejido blando. En los sistemas de fotón dual, sin embargo, un isótopo que emitía energía en 2 distintos picos fotoeléctricos, o 2 isótopos, cada uno emitiendo energía de fotones en picos fotoeléctricos separados y distintos, eran utilizados. Cuando el haz pasaba a través de la región corporal con hueso y tejido blanco, la atenuación del haz de fotones ocurría en ambos picos de energía. Si un pico de energía era atenuado preferentemente por el hueso, las contribuciones de tejido blando a la atenuación del haz podían ser matemáticamente sustraídas. Como en la absorciometría de fotón único, las contribuciones remanentes de la atenuación del haz por el hueso eran cuantificadas y luego comparadas con estándares creados de huesos secos. La habilidad para separar el hueso de los tejidos blandos finalmente permitió la cuantificación de la densidad ósea en aquellas áreas del esqueleto rodeadas por masas grandes o irregulares de tejido blando, notablemente la columna vertebral y el fémur proximal. DPA fue también utilizada para determinar la densidad ósea corporal total. El desarrollo de DPA y sus aplicaciones a la columna vertebral, el fémur proximal y el cuerpo total es atribuido a varios grupos de investigación.
El isótopo utilizado más comúnmente en la absorciometría de fotón dual era 153Gd, que emitía naturalmente energía de fotones en 2 picos fotoeléctricos, 44 y 100 keV. En el pico fotoeléctrico de 44 keV, el hueso atenuaba preferencialmente la energía de fotones. Los haces de fotones atenuados eran detectados por un detector de cintilación de NaI y cuantificados después de pasar a través de analizadores de altura de pulso ajustados a 44 y 100 keV. El soporte blindado para la fuente de 153Gd, el cual era colimado y equipado con un disparador que era operado por computadora, se movía en tándem con el detector de NaI en una ruta de escaleno rectilínea sobre la región de interés. Un cálculo punto por punto de la densidad ósea en la ruta de escaneo era realizado.
Los estudios de densidad ósea con DPA de la columna lumbar eran realizados con el haz de energía de fotones pasando en una dirección posterior a anterior (PA). Debido a la dirección del haz, el cuerpo vertebral y los elementos posteriores eran incluidos en la ruta de escaneo. Los procesos transversos eran eliminados. Esto resultó en la medición combinada de hueso cortical y trabecular, o en una medición integral que incluía el cuerpo vertebral más trabecular rodeado por su cubierta cortical y los elementos posteriores altamente corticales. Los resultados eran reportados con una densidad de área en g/cm2. La densidad mineral ósea del fémur proximal fue también una densidad de área que fue obtenida con el paso del haz en la dirección posterior a anterior.
Los estudios DPA de la columna requerían aproximadamente 30 minutos para completarse. Los estudios del fémur proximal tomaban de 30 a 45 minutos. Los estudios de densidad corporal total con DPA requerían 1 hora. La dosis de radiación dérmica eran bajas durante los estudios de columna o fémur proximal, a 15 mrem. La exactitud de las mediciones DPA de la columna iban de 3% a 6& y para el fémur proximal de 3% a 4%. La precisión de las mediciones de la densidad ósea de la columna era de 2% a 4% y alrededor de 4% para el cuello femoral.
La absorciometría de fotón dual fue considerada un importante avance de la absorciometría de fotón único, porque permitió la cuantificación de la densidad ósea en la columna y en el fémur proximal. Sin embargo, DPA tenía varias limitaciones. El mantenimiento de la maquina era costoso; la fuente de 153Gd debía ser reemplazada cada año a un costo superior a los $5,000 dólares estadounidenses. También debía considerarse que a medida que la fuente radiactiva decaída, los valores obtenidos con DPA se incrementaban tanto como 0.6% al mes, en tanto que con el reemplazo de la fuente, los valores podían caer tanto como 6.2%. Aunque se desarrollaron fórmulas matemáticas para compensar por el efecto del deterioro de la fuente, seguía siendo un motivo de preocupación, afectando potencialmente tanto la exactitud como la precisión. La precisión de 2%-4% para mediciones DPA de la columna y el fémur proximal limitaron su aplicación para detectar cambios en la densidad ósea. Con una precisión del 2%, un cambio de al menos 5.5% del valor base debía ser visto antes de poder estar seguro con un nivel de confianza del 95% de que había ocurrido un cambio. Con una precisión del 4%, este valor se incrementada a 11.1%. Con un nivel de confianza de 80%, el cambio requerido para valores de precisión de 2% y 4% eran 3.6% y 7.2%, respectivamente. Esto significó que los estudios DPA de densidad ósea no mostrarían cambios significativos por hasta 5 años, lo que era un período demasiado largo para ser clínicamente útil.
En los estudios DPA de densidad ósea en columna, en los cuales el haz de fotones pasaba en una dirección PA, el cuerpo vertebral altamente trabecular no podía ser separado de sus elementos posteriores más corticales. Adicionalmente, la cubierta cortical del cuerpo vertebral no podía ser separada de su interior trabecular. Las calcificaciones en el tejido blando o en la aorta abdominal atenuaban el haz, elevando falsamente los valores de densidad ósea. Los cambios artríticos en los elementos posteriores de la columna también afectaban la medición. Los estudios DXA de la columna no son inmunes a estos efectos tampoco, pero los estudios DXA laterales de columna pueden ser realizados para superar estas limitaciones. Los estudios de la columna en la proyección lateral nunca estuvieron disponibles con DPA.
La habilidad para hacer predicciones de fractura específicas a un sitio en la columna y el fémur proximal, o predicciones de riesgo global de fractura con la absorciometría de fotón dual fue establecida en pruebas prospectivas. Como SPA, DPA se realiza raramente en los países desarrollados, debido a la disponibilidad de DXA y sus mejoras tecnológicas.
Absorciometría de rayos-X de energía dual
Los principios subyacentes de la absorciometría de rayos-X de energía dual (DXA, por sus siglas en inglés) son los mismos que aquellos de la absorciometría de fotón dual. Con DXA, sin embargo, la fuente de isótopo radioactivo ha sido substituida con un tubo de rayos-X. Hay varias ventajas de las fuentes de rayos-X sobre los isótopos radioactivos: no hay deterioro de la fuente que pueda requerir un costoso reemplazo de la fuente radioactiva; similarmente, no hay preocupación de variación en los valores de un paciente debido a deterioro de la fuente. La mayor intensidad de la fuente o flujo de fotones producido por el tubo de rayos-X y el punto focal más pequeño permiten una mejor colimación del haz, resultando en menos traslape de dosis entre líneas de escaneo y mayor resolución de la imagen. Los tiempos de escaneo son menores y la precisión es mejorada.
Dado que los tubos de rayos-X producen un haz que abarca un amplio rango de energías de fotones, el haz debe ser angostado de alguna manera a fin de producir los 2 picos fotoeléctricos distintos, necesarios para separar el hueso del tejido blando. Los principales fabricantes de absorciómetros de rayos-X de energía dual han logrado esto mediante el uso de filtros de borde K de tierras raras para producir 2 picos fotoeléctricos o mediante el uso de una fuente de poder de pulsos para el tubo de rayos-X para crear el mismo efecto.
Los filtros de borde K producen un haz de rayos-X con un alto número de fotones en un rango específico. El rango de energía que se desea es el rango de energía que está justo arriba del borde de absorción K del tejido en cuestión. El borde K es la energía ligadora del electrón del nivel K. Este nivel de energía varía de un tejido a otro. La importancia del borde K es que en energías de fotón justo arriba de este nivel, la transmisión de fotones a través del tejido en cuestión cae dramáticamente; esto es, los fotones son atenuados al máximo en este nivel de energía. Por lo tanto, para separar tejido óseo de tejido blando de una manera cuantificable, la energía del haz de fotones debe estar justo sobre el borde K del hueso o del tejido blando para una atenuación máxima. GE Healthcare utiliza un filtro de cerio en sus dispositivos centrales que tiene un borde de absorción del nivel K a 40 keV. Un espectro de rayos-X filtrado con cerio a 80 kV contendrá 2 picos fotoeléctricos aproximadamente en 40 keV y 70 keV. El filtro de borde K de samario empleado por Norland en sus dispositivos centrales tiene un borde de absorción del nivel K a 46.8 keV. El haz de rayos-X filtrado con samario a 100 kV produce un pico de baja energía a 46.8 keV. En el sistema Norland, el pico de alta energía es variable, debido a que el sistema emplea niveles seleccionables de filtración, pero los fotones están limitados a menos de 100 keV por los 100 kV empleados. El borde K de cerio y samario resulta en un pico de baja energía que se aproxima al pico de baja energía de 44 keV de 153Gd empleado en los sistemas de fotón dual.
Los dispositivos DXA centrales de Hologic utilizan un sistema diferente para producir los 2 picos fotoeléctricos necesarios para separar el hueso del tejido blando. En lugar de emplear filtrado de borde K del haz de rayos-X, Hologic emplean pulsos alternados a la fuente de rayos-X en 70 kV y 140 kV.
La mayoría de las regiones del esqueleto (y por tanto, del cuerpo humano) son accesibles DXA (también se conoce como DEXA). Los estudios pueden realizarse en la columna tanto en la proyección anteroposterior como en la proyección lateral. Los estudios de espina lumbar obtenidos en la proyección lateral tienen la habilidad de eliminar los efectos confundidores de la calcificación distrófica en densidades medidas en la dirección PA. Los escaneos laterales también eliminan los elementos posteriores altamente corticales que contribuyen con tanto como el 47% del contenido mineral medido en la dirección PA. La utilidad de los estudios DXA lateral de espina lumbar puede estar limitada por el traslape de las costillas de L1 y L2 y el traslape pélvico de L4, más cuando se realiza en la posición decúbito lateral izquierda que en la posición supina. Las densidades óseas en el fémur proximal, antebrazo, calcáneo y cuerpo total pueden también ser medidas con DXA.
Los tiempos de escaneo son dramáticamente más cortos con DXA que en DPA. Las unidades DXA tempranas requerían aproximadamente 4 minutos para estudios de la espina lumbar PA o el fémur proximal. Los estudios de cuerpo completo requerían 20 minutos en el modo de escaneo medio y solamente 10 minutos en el modo de escaneo rápido. Las nuevas unidades DXA escanean todavía más rápido, y los estudios de la columna AP o el fémur proximal requieren menos de 1 minuto para realizarse.
Los valores obtenidos con los estudios de rayos-X de energía dual del esqueleto están latamente correlacionados con valores de estudios previos realizados con absorciometría de fotón dual. Consecuentemente, la exactitud de DXA es comparable con la de DPA. Los valores DXA de columna y los valores DXA de fémur proximal de Hologic y Norland son consistentemente menores que los obtenidos con equipo DXA de los otros fabricantes importantes. Los valores obtenidos con unidades DXA de Hologic o Norland son consistentemente menores que los obtenidos con la unidad DXA de Lunar, aunque todos están altamente correlacionados entre sí. Los estudios de comparación utilizando los dispositivos DXA centrales de los 3 fabricantes, han resultado en el desarrollo de fórmulas que hacen posible convertir los valores de espina lumbar y cuello femoral obtenidos con el dispositivo de un fabricante al valor esperado con los dispositivos de otros fabricantes. No obstante, el margen de error en dichas conversiones es todavía muy alto para utilizar dichos valores en el seguimiento de un paciente en el tiempo. Dichos valores, por lo tanto, deben ser vistos solamente como aproximaciones. Otro juego de fórmulas hace posible la conversión del valor de “densidad mineral ósea” (BMD, por sus siglas en inglés) de un fabricante en la espina lumbar o cadera total, a un segundo valor llamado “densidad mineral ósea estandarizada” (sBMD, por sus siglas en inglés). El sBMD es siempre reportado en mg/cm2, para distinguirlo del BMD del fabricante, que se reporta en g/cm2.
Tal vez el avance más significativo observado con DXA comparado con DPA es la mejora marcada en la precisión. Expresada como un coeficiente de variación, la precisión a corto plazo en sujetos normales ha sido reportada tan bajo como 0.9% para la espina lumbar PA y de 1.4% para el cuello femoral. Los estudios de precisión en el curso de 1 año han reportado valores de 1% para la espina lumbar PA y 1.7%-2.3% para el cuello femoral.
La exposición a radiación es extremadamente baja para todos los tipos es escaneos DXA. Expresada como dosis dérmica, la exposición a radiación durante estudio de espina lumbar PA o fémur proximal es solamente de 2-5 mrem. La dosis efectiva biológicamente importante o la dosis equivalente de cuerpo completo es solamente de 0.1 mrem.
DXA ha sido empleada en estudios prospectivos para predecir el riesgo de fractura. En uno de los estudios más grandes de su tipo, los estudios DXA del fémur proximal demostraron la mayor habilidad predictiva a corto plazo para fractura de cadera, comparada con mediciones en otros sitios con SPA o DPA.
Los dispositivos centrales de DXA son llamados escáneres de “haz de lápiz” o de “haz amplio” (también llamado de arreglo amplio, de abanico o fan-array). Ejemplos de escáner de haz de lápiz son Lunar DPX Plus, DPX-L, DPX-IQ, DPX-SF, DPX-A, DPX-MD, DPX-MD+ y DPX-NT, Hologic QDR 1000 y QDR 2000, y Norland XR-36, XR-46, Excell y Excell plus. Ejemplos de escáner DXA de haz amplio son Lunar Expert, Bravo, Duo, Prodigy e iDXA, y Hologic QDR 4500 A, QDR 4500 C, QDR 4500 W, QDR 4500 SL, Delphi, Discovery y Explorer. Los escáneres de haz de lápiz emplean un haz de rayos-X colimado o angostado (angosto como un lápiz) que se mueve en tándem en un patrón rectilíneo con los detectores. Los escáneres de haz amplio utilizan un haz mucho más amplio o en forma de abanico y un arreglo de detectores, de manera que una línea de escaneo entera puede ser cuantificada instantáneamente. Los tiempos de escaneo son reducidos a tanto como 30 segundos para un estudio PA de la espina lumbar. La resolución de imagen está también mejorada con los escáneres de haz amplio, lo que ha creado una nueva aplicación para el análisis computarizado del escaneo de densitometría ósea llamado absorciometría de rayos-X morfométrica (MXA, por sus siglas en inglés). Con MXA, las imágenes de la columna obtenidas en la proyección lateral pueden ser usadas para el análisis computarizado de las dimensiones vertebrales y el diagnóstico de fractura vertebral. Los escáneres de haz amplio también han sido desarrollados para imágenes de espina lateral en su totalidad, para permitir una mejora visual del tamaño y forma vertebrales. Ejemplos de escáneres con esta capacidad con Hologic Delphi y Lunar Prodigy.
DXA ha reemplazado efectivamente a DPA tanto en la investigación como en la práctica clínica. Los menores tiempos de escaneo, la resolución de imagen mejorada, la menos dosis de radiación, la precisión mejorada, la aplicación a más sitios del esqueleto y el menor costo de operación con DXA han relegado a DPA a un lugar de honor en la historia de la densitometría.
DXA periférica
La tecnología de rayos-X de energía dual es también empleada en equipos portátiles, dedicados a la medición de uno o 2 sitios apendiculares. Como tales, estos equipos están caracterizados como equipos periféricos o equipos pDXA, por sus siglas en inglés. Dado que estos equipos emplean rayos-X de energía dual, no requieren un bajo de agua o gel equivalente al tejido rodeando la región del esqueleto a ser estudiada. Como consecuencia, son más fáciles de mantener y usar que los equipos SXA. Ejemplos de unidades pDXA son Lunar PIXI, Norland pDEXA y Norland Apollo, Schick accuDEXA y Osteometer DexaCare DTX-200 y G4.
Absorciometría de rayos-X de energía única
La absorciometría de rayos-X de energía única (SXA, por sus siglas en inglés) es la contraparte basada en rayos-X de la absorciometría de fotón único, tanto como la absorciometría de rayos-X de energía dual es la contraparte basada en rayos-X de la absorciometría de fotón dual. Las unidades SXA fueron utilizadas para medir la densidad ósea en el radio distal, en el cúbito y en el calcáneo. Como sus contrapartes DXA, las unidades SXA no utilizaban isótopos radioactivos, pero requieren un baño de agua o un gel equivalente al tejido rodeando la región del esqueleto a ser medida. La exactitud y precisión de SXA era comparable a SPA. Con el desarrollo de equipos DXA portátiles para la medición de densidad ósea en antebrazo y calcáneo, que no requieren un baño de agua o gel, SXA se ha vuelto obsoleto, justo como su predecesor SPA.
Tomografía computarizada cuantitativa
Aunque la tomografía computarizada cuantitativa (QCT, por sus siglas en inglés) en una técnica absorciométrica de fotones como SPA, SXA, DPA y DXA, es única porque proporciona una medición tridimensional o volumétrica de la densidad ósea y una separación espacial del hueso trabecular del cortical. En 1976 se desarrolló un escáner de tomografía computarizada (CT, por sus siglas en inglés) cuantitativo periférico dedicado, utilizando 125I para mediciones del radio y poco más tarde se adaptaron escáneres CT comerciales para la valoración cuantitativa de la densidad ósea de la columna vertebral, siendo este el acercamiento con uso más amplio en varios países, aunque unidades CT dedicadas a la medición del esqueleto periférico, o unidades pQCT, se utilizan todavía en los centros clínicos.
Los estudios QCT de la columna utilizan un estándar de referencia o fantasma que es escaneado simultáneamente con el paciente. El fantasma contiene una concentración variada de K2HPO4 y es colocado bajo el paciente durante el estudio. Se requiere una vista de exploración para la localización y luego se hace una medición de una rebanada de 8-10 mm de espesor a través del centro de 2 o más cuerpos vertebrales que son generalmente seleccionados de /12 a L3. Una región de interés dentro de la porción anterior del cuerpo vertebral es analizada para densidad ósea y es reportada como mg/cm3 de K2HP4 equivalentes. Esta región de interés es cuidadosamente colocada para evitar la cubierta cortical del cuerpo vertebral. El resultado es una densidad trabecular tridimensional diferente a las densidades mixtas cortical y trabecular bidimensionales de área, reportadas con estudios PA de la columna utilizando DPA o DXA.
Un estudio de la columna con QCT requiere unos 30 minutos. La dosis de radiación dérmica es generalmente de 100-300 mrem. Esto sobreestima la dosis efectiva biológicamente importante, porque solamente una pequeña porción de médula es irradiada durante un estudio QCT de la columna. La dosis efectiva o la dosis equivalente de cuerpo completo está generalmente en el rango de 3 mrem (30 µSv). El escaneo localizador que precede al estudio QCT adiciona 3 mrem a la dosis efectiva. Estos valores son bastante aceptables en el contexto de radiación natural de fondo (aproximadamente unos 20 mrem/mes). Las unidades CT antiguas, que por su diseño no podían utilizar ajustes de bajo kVp para los estudios QCT, pueden administrar dosis 3-10 veces mayores.
La exactitud de QCT para mediciones de la densidad ósea de la columna puede ser afectada por la presencia de grasa en la médula. La grasa en la médula se incrementa con la edad, resultando en un error que se incrementa en la exactitud de las mediciones QCT de la columna en los pacientes ancianos. La exactitud de QCT ha sido reportada en el rango de 5%-15%, dependiendo de la edad del paciente y del porcentaje de grasa en la médula. La presencia de grasa en la médula resulta en una subestimación de la densidad ósea en el paciente joven de cerca de 20 mg/cm3 y tanto como 30 mg/cm3 en el anciano. El error introducido por la grasa de la médula puede ser parcialmente corregido por aplicación de datos de grasa en la médula vertebral con la edad desarrollados por Dunnill y otros en 1967. En un intento por eliminar el error inducido por la grasa de la médula, se desarrolló la QCT de energía dual (DEQCT, por sus siglas en inglés), que claramente reduce el error introducido por la presencia de la grasa de la médula hasta un valor de 1.4% en estudios cadavéricos. In vivo, la exactitud con DEQCT es 3%-6%. La dosis de radiación con DEQCT se incrementa unas 10 veces comparadas con la QCT normal o de energía única (SEQCT, por sus siglas en inglés), pero la precisión no es tan buena. La precisión de SEQCT para mediciones vertebrales en manos expertas es de 2%-3% y para DEQCT es de 3%-5%.
La medición de densidad ósea en el fémur proximal con QCT ha aumentado su disponibilidad en años recientes. Utilizando tanto unidades QCT dedicadas cono unidades CT estándar, os investigadores han empleado QCT para mediciones del fémur proximal, empleando en ocasiones aplicaciones de software que proporciona valores equivalentes a DXA. El software de análisis estructural de QCT del fémur y cadera también ha sido desarrollado.
QCT de la columna ha sido utilizado en estudios de fracturas osteoporósicas prevalentes y es claro que dichas mediciones pueden distinguir a los individuos osteoporósicos de los individuos normales tan bien o aún mejor que DPA. Las fracturas son raras con valores sobre 110 mg/cm3 y extremadamente comunes por debajo de 60 mg/cm3. Dado que QCT puede aislar y medir el hueso trabecular, el cual es más activo metabólicamente que el hueso cortical, las tasas de cambio en los estados de enfermedad observadas con las mediciones QCT de columna tienden a ser mayores que aquellas observadas con estudios PA de columna, realizados con DPA o DXA. Esta magnitud mayor de cambio, parcialmente compensa los efectos de la precisión más pobre observada con QCT comparada con DXA. Las correlaciones entre mediciones de densidad ósea de columna entre QCT y sitios esqueléticos medidos con otras técnicas son estadísticamente significativas, pero muy débiles para permitir la predicción exacta de densidad ósea en otro sitio a partir de mediciones de la columna con QCT. Esto no difiere, sin embargo, de intentar utilizar BMD en la columna, obtenida con DXA para predecir BMD en otros sitios del esqueleto.
QCT periférica
La QCY periférica (pQCT, por sus siglas en inglés) se está volviendo ampliamente disponible. Los equipos pQCT son utilizados primariamente para mediciones de densidad ósea en el antebrazo. Como los escaneo QCT de la columna, pQCT hace posible las mediciones tridimensionales o volumétricas de la densidad ósea en el antebrazo, lo cual puede ser particularmente útil cuando el tamaño del hueso está cambiando, como en las poblaciones pediátricas. Ejemplos de equipos pQCT comerciales son Stratec XCT 2000L y XCT 3000.
Tomografía computarizada cuantitativa de alta resolución
La tomografía computarizada cuantitativa de alta resolución (HS-QCT, por sus siglas en inglés) es una nueva generación de QCT en la cual la resolución espacial ha sido incrementada para permitir la imagen de trabéculas individuales. Las mediciones volumétricas de BMD pueden todavía ser obtenidas con HS-QCT justo como se hace con QCT. Sin embargo, HS-QCT puede emplearse también para cuantificar los parámetros estructurales del número trabecular, el espaciado trabecular, el grosor trabecular y la distribución. Actualmente, HS-QCT está limitado al radio y tibia por lo que es más correctamente caracterizado como HS-pQCT, por sus siglas en inglés Con este acercamiento, se puede obtener un tamaño de voxel (pixel volumétrico) isotrópico nominal de 82 µm.
En los trabajos tempranos, se demostró que los parámetros estructurales de HS-pQCT estaban altamente correlacionados con los parámetros estructurales de biopsias óseas de la cresta ilíaca, valoradas con µCT. HS-pQCT fue empleada para obtener mediciones tridimensionales de la densidad ósea así como parámetros estructurales en el radio distal y la tibia distal en mujeres premenopáusicas y postmenopáusicas, realizándose también mediciones DXA de la espina lumbar y el cuello femoral. La precisión a corto plazo fue valorada en 15 mujeres sanas que se sometieron a 3 escaneos HS-pQCT de radio y tibia. La precisión de los parámetros estructurales de número trabecular (TbN, por sus siglas en inglés), espesor trabecular (TbTh, por sus siglas en inglés), espaciado trabecular (TbSp, por sus siglas en inglés), desviación estándar del espaciado trabecular (TbSpSD, por sus siglas en inglés) y espesor cortical (CTh, por sus siglas en inglés) estuvieron en el rango de 0.9% a 4.4% tanto en radio como en tibia distales. En las mujeres postmenopáusicas en ambos sitios esqueléticos, la densidad trabecular y la densidad cortical medidas por HS-pQCT fueron significativamente menores que en las mujeres premenopáusicas. Las mujeres postmenopáusicas también tuvieron número y espesor trabeculares significativamente más bajos y una mayor separación trabecular. De las mujeres categorizadas como osteopénicas en base al registro T de DXA en la espina lumbar o en el cuello femoral, los parámetros HS-pQCT de volumen de fractura de hueso trabecular (BV/TV, por sus siglas en inglés) y TbSpSD fueron significativamente diferentes en las mujeres con fracturas de columna, comparadas con las mujeres sin fractura, mientras que BMD en la columna y en el cuello femoral medidos por DXA no lo fueron.
HR-pQCT de radio y tibia distales también han sido usados para evaluar la densidad volumétrica y arquitectura en un estudio con mujeres que podían o no presentar fracturas de columna, con seguimiento por 13 años. Estas mujeres también se sometieron a DXA del radio ultradistal y del fémur proximal. Comparadas con controles de la misma edad, las mujeres con fracturas tuvieron menores BV7TV, CTh, TbN y TbSp, así como un incremento en TbSpSD. Después de ajustar para el BMD medido con DXA, hubo una tendencia hacia una diferencia significativa continua para TbN, TbSp y TbSpSD. En la tibia, aún después de ajustar para el BMD obtenido con DXA, TbTh continuó significativamente disminuido en las pacientes con fractura, comparadas con los controles.
Una característica atractiva de HS-pQCT es que proporciona tanto densidad ósea volumétrica como parámetros estructurales. Al ser QCT, expone al paciente a radiación ionizante, pero la exposición es menos de 5 µSv. Los tiempos de escaneo son también aceptablemente cortos en aproximadamente 3 minutos. Existe equipo disponible comercialmente para realizar HS-pQCT, pero su uso se restringe casi por completo a procedimientos de investigación.

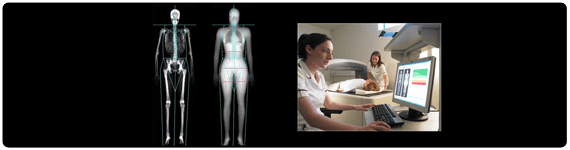

Estoy cursando la carrera de nutriologa y una de las materias más importantes es la evaluacion del estado nutricio, en donde se incluyen tecnicas como la DEXA. Gracias a su blog ahora entiendo mejor como funciona el equipo, y esto es importante porque debemos conocer el principio por el que operan los equipos, en principio para saber si operan correctamente y tambien porque es muy comun que los pacientes pregunten sobre el funcionamiento y los riesgos de someterse a una prueba, sobre todo cuando ven un equipo que no conocen. Esto me ha pasado en las clinicas en donde he estado en mis prácticas con mucha frecuencia. Gracias.
Hola Georgina,
En efecto, la técnica DEXA se utilizada ampliamente en muchos centros de salud, aunque el elevado costo del equipo (aun cuando es muchísimo más económico que otros como el CT o el MRI) ha dificultado su aplicación a nivel general, teniendo que conformarse en muchas ocasiones con mediciones antropométricas, que con las formulas adecuadas son bastante útiles (pronto incluiremos algunos articulos sobre antropometría, pues nos los han solicitado varias personas).
Muchos de nosotros somos nutriólogos, incluyendo el coordinador general de Nutrición Personalizada, quien es egresado de la Universidad Iberoamericana, por lo que nos da mucho gusto que otros nutriólogos sean lectores del blog. Confiamos en que la retroalimentación constante nos ayude a todos a ser mejores en nuestra profesión.