 La hipertrigliceridemia se refiere a una medición de triacilgliceroles (triglicéridos) en plasma y en ayuno, típicamente arriba del percentil 95 para edad y sexo, aunque anormalidades cuantitativas o cualitativas en lipoproteínas adicionales también pueden estar presentes.
La hipertrigliceridemia se refiere a una medición de triacilgliceroles (triglicéridos) en plasma y en ayuno, típicamente arriba del percentil 95 para edad y sexo, aunque anormalidades cuantitativas o cualitativas en lipoproteínas adicionales también pueden estar presentes.
Los pacientes pueden fluctuar entre estados hipertrigliceridémicos: con el estrés metabólico apropiado, la hipertrigliceridemia leve o moderada puede deteriorarse hasta una hipertrigliceridemia severa.
Las concentraciones elevadas de triglicéridos en plasma contribuyen a un mayor riesgo de enfermedad cardiovascular, tanto de manera directa como por su asociación a otros factores de riesgo como obesidad, síndrome metabólico, biomarcadores pro-inflamatorios y pro-trombóticos, así como diabetes mellitus (tipo 2). Un incremento en el riesgo de pancreatitis aguda es una consideración adicional cuando el nivel de triglicéridos es muy alto (típicamente > 10 mmol/l).
Las dos principales fuentes de triglicéridos en plasma son las exógenas (de la grasa en la dieta) que son transportados en los quilomicrones, y las endógenas (del hígado) que son transportados en las partículas de lipoproteínas de muy baja densidad (VLDL, por sus siglas en inglés). En los capilares dentro de los tejidos adiposo y muscular estas lipoproteínas y quilomicrones son hidrolizados por lipoproteinlipasa en ácidos grasos libres.
Después de una comida, más del 90% de los triglicéridos en circulación se originan en el intestino y son secretados en quilomicrones, mientras que en los periodos de ayuno predominan los triglicéridos endógenos, secretados por el hígado como VLDL. El incremento en plasma de lipoproteínas ricas en triglicéridos resulta del aumento en la producción en hígado e intestino (por medio de rutas secretoras y sintéticas estimuladas) o a través de una disminución en el catabolismo periférico (principalmente por una reducción en la actividad de lipoproteinlipasa).
Existen 2 tipos de hipertrigliceridemia, la primaria y la secundaria. En la era postgenómica (posterior a la elucidación de la secuencia del genoma humano) un sistema de clasificación para los desórdenes de triglicéridos debe estar basado en diagnosis molecular, pero una base molecular para la hipertrigliceridemia primaria se ha encontrado en menos del 5% de los casos, mientras que para los casos secundarios no se ha encontrado un componente reproducible de susceptibilidad genética.
La mayoría de los pacientes con hipertrigliceridemia tiene por lo menos un factor secundario; sin embargo, no todas las personas con exposición equivalente a factores secundarios desarrollan dislipidemia igualmente severa lo que sugiere un papel para la susceptibilidad endógena primaria monogénica o poligénica.
Se ha sugerido el uso de 4 estratos de triglicéridos en el contexto de valoración de riesgo de enfermedad cardiovascular: normal (< 1.7 mmol/l), ligeramente alto (1.7-2.3 mmol/l), alto (2.3-5.6 mmol/l) y muy alto (> 5.6 mmol/l). El esquema alternativo, ahora en desuso, es el sistema Fredrickson, que emplea tipos numéricos.
Hipertrigliceridemia primaria
Los quilomicrones son normalmente removidos con rapidez del plasma por la lipoproteinlipasa con apolipoproteína (apo) C-II como cofactor. La quilomicronemia familiar (hiperlipoproteinemia tipo 1 en el sistema Fredrickson) y la hiperlipidemia mixta primaria (hiperlipoproteinemia tipo 5) se caracterizan por la presencia patológica de quilomicrones después de un ayuno de 12 a 14 horas.
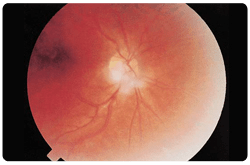
Las características clínicas observadas tanto en la quilomicronemia familiar como en la hiperlipidemia mixta primaria incluyen xantoma eruptivo, lipemia retinal, hepatoesplenomegalia, síntomas neurológicos focales como irritabilidad y dolor epigástrico recurrente con riesgo incrementado de pancreatitis.
Las muestras de plasma lipémico desarrollan un supernadante cremoso cuando se refrigeran (4°C) toda la noche; cuando se prueba el plasma, las medidas de triglicéridos en ayuno están típicamente por arriba de 10 mmol/l en casos de quilomicronemia familiar o hiperlipidemia mixta primaria.

Características distintivas clave de la quilomicronemia familiar y de la hiperlipidemia mixta primaria incluyen la manifestación inicial durante la niñez para la primera, y en la adultez para la segunda; deficiencia bioquímicamente probada de lipoproteinlipasa, actividad apo CII o mutaciones homocigosas del gen en el caso de quilomicronemia familiar, con deficiencia funcional menos severa y detección poco frecuente de mutaciones del gen en la hiperlipidemia mixta primaria; prevalencia poblacional mucho menor en la primera (alrededor de 1:106) que en la segunda (alrededor de 1:103); presencia frecuente de factores secundarios en la segunda; y una mayor elevación de colesterol total en la hiperlipidemia mixta primaria relativa a la quilomicronemia familiar.
En el diagnóstico bioquímico, la quilomicronemia familiar presenta una pérdida de actividad lipoproteinlipasa en plasma colectada después de una dosis intravenosa de heparina (sin embargo, pocos laboratorios realizan esta prueba en la actualidad).
La hipertrigliceridemia familiar (hiperlipoproteinemia tipo 4) se define por la elevación aislada de VLDL, que no son tan ricas en triglicéridos como los quilomicrones. Este desorden familiar tiene una prevalencia poblacional de entre 5 y 10%. Su base molecular se desconoce en buena media pero muy posiblemente sea poligénica, requiriendo un factor secundario para su expresión.
Típicamente, los pacientes con este desorden tienen mediciones de triglicéridos en plasma moderadamente elevadas (3-10 mmol/l), frecuentemente con bajos niveles de lipoproteínas de alta densidad-colesterol (HDL-C por sus siglas en inglés).
La hipertrigliceridemia familiar está asociada con incremento en el riesgo de enfermedad cardiovascular, obesidad, resistencia a la insulina, diabetes, hipertensión e hiperuricemia.
El patrón de herencia de la hiperlipoproteinemia combinada familiar (tipo 2B) es autosómica dominante con penetrancia variable y una prevalencia poblacional del 2 al 5%. Las anormalidades en lipoproteínas son un incremento en VLDL y en lipoproteínas de baja densidad (LDL, por sus siglas en inglés) con una disminución en DHL, asociadas con un perfil anormal de lipoproteínas en por lo menos un pariente en primer grado.
Las personas afectadas ocasionalmente tienen heterocigosidad obligada por mutaciones en los genes LPL o APOC3, pero las bases moleculares subyacentes de la hiperlipoproteinemia combinada familiar se desconocen casi por completo. Un gen recientemente definido como posible causante de este desorden es USF1, que codifica un factor estimulatorio hacia el extremo 5’ (upstream) aunque varios otros genes (incluyendo APOA5 y APOC3) han sido identificados de manera variable como causantes.
Finalmente, la disbetalipoproteinemia familiar (hiperlipoproteinemia tipo 3) tiene una prevalencia poblacional de 1-2 en 20,000 y la principal anormalidad observable en lipoproteína es un incremento en los remanentes de lipoproteína ricos en triglicéridos, también conocidos como lipoproteínas de intermedia densidad o β-VLDL que producen una elevación equimolar de las medidas de colesterol total y triglicéridos en plasma.
Las personas con este desorden típicamente son homocigóticas para la isoforma E2 con defecto de unión del gen APOE, que difiere de la isoforma común E3 por una substitución de cisteína por la arginina normal en el residuo 158 en el dominio de unión del receptor. La expresión fenotípica, sin embargo, usualmente requiere factores de acompañamiento como obesidad, diabetes tipo 2 o hipotiroidismo.
Los niveles en plasma de LDL son bajos debido al procesamiento interrumpido de VLDL. Un índice VLDL-C:triglicéridos elevado y la homocigosidad E2/E2 son diagnósticos. Las personas afectadas con frecuencia presentan xantoma tuberosa o tuberoeruptiva en las superficies extensoras de las extremidades, xantoma plano o en las líneas palmares así como un incremento en el riesgo de enfermedad cardiovascular.
Hipertrigliceridemia secundaria
Algunas condiciones metabólicas están frecuentemente (aunque no universalmente) asociadas con resultados de triglicéridos altos, sugiriendo que las personas que desarrollan hipertrigliceridemia secundaria podría tener un sutil defecto metabólico hereditario que confiere susceptibilidad. La obesidad es probablemente el estresante metabólico más frecuentemente asociado con hipertrigliceridemia, aunque asociaciones con diabetes tipo 2 pobremente controlada y el consumo excesivo de alcohol también son comunes.
Las personas con exceso de tejido adiposo presentan con frecuencia niveles elevados de triglicéridos y bajos de HDL-C- Aproximadamente el 80% de los hombres con circunferencia de cintura de 90 cm o más y un nivel de triglicéridos en plasma de 2 mmol/l o más, típicamente presentan una tríada metabólica de marcadores no tradicionales de enfermedad cardiovascular: hiperinsulinemia y niveles elevados de apo B y partículas pequeñas y densas de LDL. Esta tríada puede incrementar el riesgo de enfermedad cardiovascular hasta 20 veces.
El deterioro en la habilidad de la insulina para estimular la captación de glucosa y la compensación inadecuada para la insensibilidad a la insulina son la base de la diabetes tipo 2. Más aun, entre las personas insulinoresistentes sin diabetes tipo 2 la hiperinsulinemia está asociada con un cúmulo de anormalidades metabólicas llamadas síndrome metabólico.
Este síndrome, visto en personas con obesidad central, predice fuertemente el surgimiento futuro de diabetes tipo 2. Se caracteriza por intolerancia a la glucosa, dislipidemia (específicamente triglicéridos > 1.7 mmol/l y concentración baja de HDL-C) e hipertensión.
La hipertrigliceridemia, tanto en el síndrome metabólico como en la diabetes tipo 2, resulta de un incremento en las concentraciones en plasma de VLDL, con o sin quilomicronemia; deficiente actividad de lipoproteinlipasa; incremento en la actividad de la proteína de transferencia de colesteril ester (CETP, por sus siglas en inglés); y un incremento en el flujo de ácidos grasos libres al hígado.
Un hígado graso está frecuentemente asociado con hipertrigliceridemia en personas con obesidad y resistencia a la insulina.
La hipertrigliceridemia asociada con el consumo de alcohol resulta principalmente de un incremento de VLDL en plasma, con o sin quilomicronemia. En algunos consumidores de alcohol, las mediciones de triglicéridos en plasma pueden permanecer dentro del rango normal, debido a un incremento adaptativo en la actividad lipolítica. Sin embargo, el alcohol también puede deteriorar la lipolisis, especialmente cuando un paciente tiene una deficiencia funcional pre-existente de lipoproteinlipasa, que deriva en un marcado incremento en los triglicéridos en plasma.
Aunque el nivel elevado de LDL-C es la anormalidad dominante, el síndrome nefrótico también está caracterizado por incrementos en lipoproteínas conteniendo apo B, incluyendo VLDL. Los mecanismos que rigen la compleja relación entre enfermedad renal y el metabolismo de lipoproteínas probablemente incluyen sobreproducción por el hígado, que a su vez incrementa la síntesis de albúmina para compensar por la pérdida renal de proteína. La uremia está asociada con una elevación en VLDL, lo que refleja deterioro en la lipolisis, posiblemente por el efecto tóxico de los metabolitos urémicos.
Durante el tercer trimestre de embarazo, los niveles de triglicéridos en plasma normalmente se elevan hasta 3 veces, pero este incremento fisiológico de triglicéridos tiene una pequeña consecuencia clínica. Los incrementos marcados en triglicéridos también resultan, sin embargo, cuando la actividad de lipoproteinlipasa está comprometida. Aunque la quilomicronemia durante el embarazo es poco común, puede complicarse por pancreatitis, lo que puede ser fatal tanto para la madre como para el feto.
El desorden llamado hígado graso no alcohólico refleja el incremento en la prevalencia de obesidad, resistencia a la insulina y síndrome metabólico. Entre los pacientes afectados, hasta un tercio de ellos puede también presentar hepatitis esteatótica no alcohólica. Lipotoxicidad, estrés oxidativo, citocinas y los mediadores pro-inflamatorios contribuyen a la progresión de esteatosis a hepatitis esteatótica no alcohólica.
Los triglicéridos elevados y niveles disminuidos de HDL-C son los componentes que definen la dislipidemia en el desorden de los hígado graso no alcohólico. Pequeños estudios han indicado que el tratamiento con estatinas (dentro de los inhibidores de la HMG-CoA reductasa) es más efectivo que el de los fibratos (sustancias químicas derivadas del ácido fíbrico ó ácido clorofenoxiisobutírico) para corregir la dislipidemia.
Aunque el hipotiroidismo está usualmente asociado con concentraciones elevadas de LDL, los triglicéridos también pueden estar elevados. Las paraproteinemias (hipergammaglobulinemia –en macroglobulinemia-, mieloma, linfoma y leucemias linfocíticas) y los desórdenes autoinmunes (lupus eritematoso sistémico) también pueden causar hipertrigliceridemia, probablemente a través de una interferencia inmunomediada de la lipolisis.
Muchos medicamentos pueden incrementar las concentraciones de triglicéridos, entre los que destacan corticoesteroides, estrógenos (especialmente aquellos tomados oralmente), tamoxifeno, antihipertensores (β-bloqueadores no cardioselectivos, tiazidas), isotretinoina, resinas ligadoras de ácidos biliares, ciclofosfamida, regímenes antirretrovirales (especialmente para infecciones VIH) y medicamentos psicotrópicos (fenotiazinas, y antipsicóticos de segunda generación).
Si un medicamento se considera causa de hipertrigliceridemia, las indicaciones para el mismo deben ser revisadas. Si reducciones en la dosis, cambios en la ruta de administración o la substitución por otra clase de medicamento no son prácticos, entonces las marcadas elevaciones de triglicéridos deben ser tratadas con dieta o agentes farmacológicos.
Los pacientes tomando terapia antirretroviral altamente activa, particularmente inhibidores de proteasa, con frecuencia experimentan lipodistrofia, resistencia a la insulina y dislipidemia, estimándose que hasta el 80% y el 50% de los pacientes desarrolla hipertrigliceridemia e hipercolesterolemia, respectivamente.
La terapia retroviral de combinación altamente activa se ha asociado con un incremento de 26% en el riesgo relativo de enfermedad cardiovascular. Ritonavir y liponavir están más fuertemente asociados con dislipidemias; los inhibidores de 3-reverso-transcriptasa, el nucleósido stavudine y el nonucleósido neviparina y efavirenz menos consistentemente. Con frecuencia, los niveles de triglicéridos pueden mejorar cuando se cambian los agentes (si la eficacia antirretroviral no se ve comprometida).
Los medicamentos antipsicóticos de segunda generación son conocidos por estar asociados con obesidad, hipertrigliceridemia, hiperglucemia y diabetes tipo 2. Clozapina y olanzapina alteran más el metabolismo; risperidona y quetiapina tienen efectos intermedios; y aripiprazol y ziprasidona presentan los menores efectos.
Los desordenes psiquiátricos, debido a los estilos de vida asociados, pueden también predisponer a aquellas personas afectadas a alteraciones metabólicas. Los pacientes tomando antipsicóticos de segunda generación deben ser monitoreados regularmente (cada 8 a 12 meses) por ganancia de peso y cambios en niveles en plasma de glucosa y lipoproteína en ayuno.
La hipertrigliceridemia moderada es un factor de riesgo para enfermedad cardiovascular, mientras que la hipertrigliceridemia severa es un factor de riesgo para pancreatitis. Aunque las reducciones de triglicéridos en plasma probablemente reducen el riesgo de enfermedad cardiovascular, la evidencia para monoterapia con fibrato es más débil que la provista por reducciones de concentraciones de LDL-C en plasma. Sin embargo, la mejore en los niveles de triglicéridos por control de factores secundarios ayudará a reducir el riesgo de enfermedad cardiovascular.
En los años por venir, la disponibilidad de nuevos tipos de tratamiento podría resultar en una evolución del tratamiento actual para tratar la elevación de triglicéridos en plasma.



INTERESANTE INFORME SOBRE LA TERAPIA COMBINADA DE HEPARINA – INSULINA PARA TRIGLICERIDEMIA .